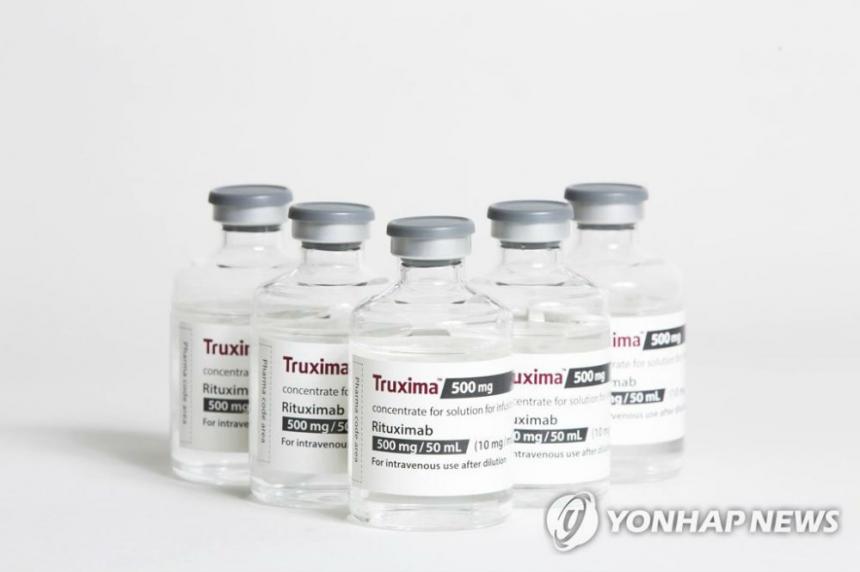
(톱스타뉴스 이창규 기자) 셀트리온[068270]의 바이오의약품 복제약(바이오시밀러) ‘트룩시마’가 미국 식품의약국(FDA) 항암제 자문위의 승인 권고를 받아 최종승인을 눈앞에 뒀다.
트룩시마는 혈액암 등의 치료에 쓰는 로슈의 맙테라(해외 판매명 리툭산) 바이오시밀러다.
셀트리온은 10일(현지 시간) 미국 매릴랜드주 FDA 화이트오크 캠퍼스에서 개최된 미국 FDA 항암제 자문위원회(Oncologic Drugs Advisory Committee)에서 트룩시마 ‘승인 권고’ 의견을 받았다고 11일 밝혔다.
자문위원회는 FDA의 독립된 자문기구로 FDA가 심사 중인 의약품의 품질, 안전성, 경제성 등에 대한 종합 의견을 제공한다.
FDA 허가 자체를 직접 결정하진 않지만 FDA 판단에 큰 영향을 끼치기 때문에 사실상 허가를 예고했다고 봐도 무방하다.
자문위원회가 트룩시마의 승인을 권고한 데 따라 셀트리온은 연내 FDA의 최종 승인을 기대하고 있다. 최종 승인 시기는 11월 말에서 12월 초로 점쳐진다.
연내 FDA 승인 시 트룩시마는 미국에서 최초로 허가받는 리툭산 바이오시밀러가 된다.
셀트리온은 트룩시마가 리툭산 바이오시밀러 시장에 처음 출시되는 ‘퍼스트무버’라는 점을 내세워 미국 시장에 안착한다는 계획이다.
현지 판매는 다국적제약사 ‘테바’가 맡으며, 구체적인 출시 일정은 아직 공개되지 않았다.



 기사를 추천하면 투표권을 받을 수 있습니다.
기사를 추천하면 투표권을 받을 수 있습니다.  모바일 모드로 보기 Go to the Mobile page.
모바일 모드로 보기 Go to the Mobile page.



 1일 투표권 3개 받기
1일 투표권 3개 받기