(톱스타뉴스 강건우 기자)
뉴시스 제공
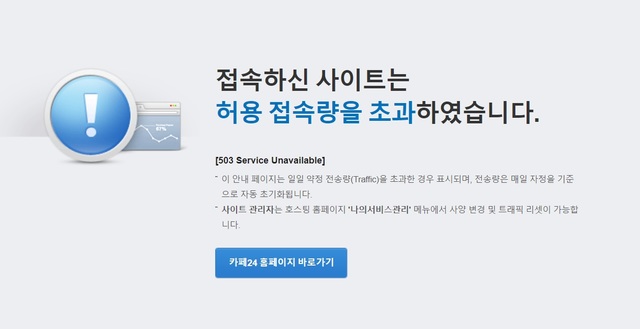
[강건우 기자] 뉴시스에 따르면 국내 코로나19 진단키트 생산업체 3곳의 제품이 미국 식품의약국(FDA)에서 사전승인을 받았다는 외교부의 발표에 한국 진단업체 홈페이지가 먹통이다.
28일 코젠바이오텍, 솔젠트, 솔젠트의 관계사 이원다이애그노믹스(EDGC)의 홈페이지는 외교부의 발표 후 몇 시간 째 허용접속량 초과로 접속이 안 되고 있다.
이날 외교부는 27일(미국 현지시간) 국내 코로나19 진단키트 생산업체 3곳의 제품이 미국 식품의약국(FDA) 긴급사용승인 절차상 사전승인을 획득했다고 밝혔다.
이번 사전승인에 따라 해당 국산 제품은 미국 시장에서 판매가 가능해졌다고 설명했다.
하지만 업체 3곳의 이름을 밝히지 않은 채 발표했다. 어떤 회사인지 알고 싶어하는 주주 및 관계자들이 각 회사의 홈페이지에 몰렸다.
이에 대해 외교부는 “이번 승인은 정식 승인은 아니고 긴급사용승인 절차상 사전승인이다. 사전승인이 어떤 의미인지는 당장 확인해주기 어렵다”며 “3개 업체가 어딘지는 정식 승인 후 FDA 홈페이지에 공개될 것”이라고 일축했다.
28일 오후 10시55분 현재 FDA에 홈페이지에 공지된 긴급사용승인(EUA, Emergency Use Authorization)받은 국내 업체는 없다.
앞서 씨젠, 코젠바이오텍, 솔젠트, 에스디바이오센서, 오상헬스케어 등이 FDA에 긴급사용승인을 신청했다.
업체들도 사전승인 받은 곳이 어딘지 몰라 혼란인 상황이다. 이들은 FDA 홈페이지에서 긴급사용승인이 확정 공지되는 것만 기다리고 있었다.
진단업체 관계자는 “그동안 계속 해외 에이전시 및 보건당국과 연락하면서 FDA에 필요한 서류를 제공·보완했던 건 업체 당사자”라며 “갑자기 들어보지도 못한 ‘사전승인’이란 표현으로 발표된 데다 어떤 업체가 받은 건지도 발표되지 않아서 우왕좌왕하고 있다”고 말했다.
업계는 조만간 긴급사용승인을 받을 것으로 전망하고 있다.

28일 코젠바이오텍, 솔젠트, 솔젠트의 관계사 이원다이애그노믹스(EDGC)의 홈페이지는 외교부의 발표 후 몇 시간 째 허용접속량 초과로 접속이 안 되고 있다.
이날 외교부는 27일(미국 현지시간) 국내 코로나19 진단키트 생산업체 3곳의 제품이 미국 식품의약국(FDA) 긴급사용승인 절차상 사전승인을 획득했다고 밝혔다.
이번 사전승인에 따라 해당 국산 제품은 미국 시장에서 판매가 가능해졌다고 설명했다.
하지만 업체 3곳의 이름을 밝히지 않은 채 발표했다. 어떤 회사인지 알고 싶어하는 주주 및 관계자들이 각 회사의 홈페이지에 몰렸다.
이에 대해 외교부는 “이번 승인은 정식 승인은 아니고 긴급사용승인 절차상 사전승인이다. 사전승인이 어떤 의미인지는 당장 확인해주기 어렵다”며 “3개 업체가 어딘지는 정식 승인 후 FDA 홈페이지에 공개될 것”이라고 일축했다.
28일 오후 10시55분 현재 FDA에 홈페이지에 공지된 긴급사용승인(EUA, Emergency Use Authorization)받은 국내 업체는 없다.
앞서 씨젠, 코젠바이오텍, 솔젠트, 에스디바이오센서, 오상헬스케어 등이 FDA에 긴급사용승인을 신청했다.
업체들도 사전승인 받은 곳이 어딘지 몰라 혼란인 상황이다. 이들은 FDA 홈페이지에서 긴급사용승인이 확정 공지되는 것만 기다리고 있었다.
진단업체 관계자는 “그동안 계속 해외 에이전시 및 보건당국과 연락하면서 FDA에 필요한 서류를 제공·보완했던 건 업체 당사자”라며 “갑자기 들어보지도 못한 ‘사전승인’이란 표현으로 발표된 데다 어떤 업체가 받은 건지도 발표되지 않아서 우왕좌왕하고 있다”고 말했다.
업계는 조만간 긴급사용승인을 받을 것으로 전망하고 있다.
<저작권자 © 톱스타뉴스 무단전재 및 재배포 금지> 2020/03/28 23:55 송고 | reporter@topstarnews.co.kr
기자의 보도 내용에 비판은 수용하며, 반론권을 보장합니다. 그러나 폭력적인 욕설이나 협박에 대해서는 합의 없는 형사 처벌을 추진하므로 유의하시기 바랍니다. 또한 톱스타뉴스의 모든 콘텐츠(영상, 기사, 사진)는 저작권법의 보호를 받습니다. 무단 전재, 복사, 배포, 유튜브 영상 제작을 금합니다. 발견 즉시 민형사상 제소합니다.
Tag
#newsis


 기사를 추천하면 투표권을 받을 수 있습니다.
기사를 추천하면 투표권을 받을 수 있습니다.  모바일 모드로 보기 Go to the Mobile page.
모바일 모드로 보기 Go to the Mobile page.



 1일 투표권 3개 받기
1일 투표권 3개 받기