(톱스타뉴스 박정민 기자) 셀트리온이 국내 특허 항소심에서 승소하며 트룩시마 판매 장애가 거의 사라졌다.
18일 셀트리온은 트룩시마의 오리지널 의약품인 리툭산(국내 판매명 맙테라)의 적응증(사용범위) 중 하나인 만성 림프구성 백혈병(CLL)에 대한 국내 특허 무효 항소심에서 승소했다고 밝혔다.
이날 판결은 바이오젠이 지난 2017년 3월 CLL 적응증 특허 무효 심결에 불복해 특허법원에 항소한 건에 대한 것으로, 특허법원은 1심 판결과 마찬가지로 무효 판결을 내렸다.
셀트리온의 트룩시마(성분명 리툭시맙)는 항체 블록버스터 의약품 리툭산의 바이오시밀러(바이오의약품 복제약)다.
지난 2016년 11월 셀트리온은 식약처로부터 트룩시마의 국내 판매허가를 획득했다.
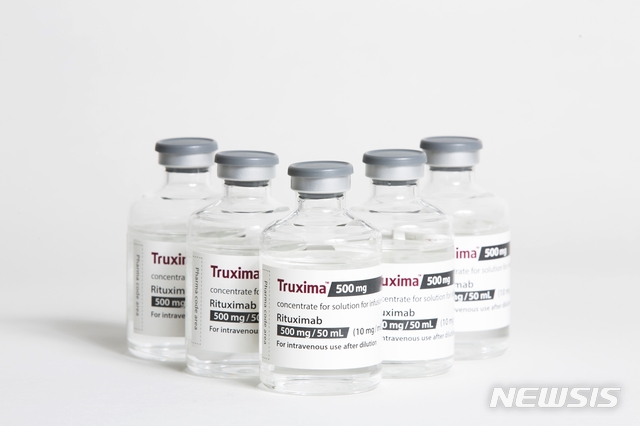
또한, 이듬해 2월 유럽 의약청(EMA), 지난해 11월 미국 식품의약국(FDA)에서도 트룩시마 판매허가를 받았다.
현재 유럽 시장의 35%를 점유하고 있다.
앞서 셀트리온은 트룩시마 제품 허가 신청 이전인 2015년 4월부터 11월까지 식약처에 등재된 바이오젠의 리툭산 관련 적응증 특허 5건에 대해 특허 무효 심판을 청구했다.
이 중 바이오젠이 CLL 적응증 특허 무효 심결에 불복해 특허법원에 항소한 1건을 제외한 나머지 4건은 2016년 8월부터 2017년 7월에 걸쳐 특허 무효가 모두 확정됐다.
셀트리온 관계자는 “특허심판원과 마찬가지로 이번 특허법원에서도 만성 림프구성 백혈병 관련 특허 무효 판결을 내려 기존 특허심판원 판결의 정당성을 다시 한번 확인할 수 있었다”라고 말했다.
이어 “현재 트룩시마 판매에 장애가 될 국내 특허 무효화 소송은 거의 마무리 된 상태로, 셀트리온은 고가의 비용 때문에 바이오의약품 치료를 받지 못했던 환자들에게 폭넓은 바이오시밀러 치료 기회를 제공할 수 있도록 판매환경을 안정적으로 조성하기 위해 적극적으로 노력하겠다”라고 덧붙였다.



 기사를 추천하면 투표권을 받을 수 있습니다.
기사를 추천하면 투표권을 받을 수 있습니다.  모바일 모드로 보기 Go to the Mobile page.
모바일 모드로 보기 Go to the Mobile page.



 1일 투표권 3개 받기
1일 투표권 3개 받기